Thermische Energie und Wärmekraftmaschinen
Grundlagen der Thermodynamik und der Kreisprozesse, Zustandsgrößen und Prozessgrößen und ihre Anwendung als Wärmekraftmaschine
Jetzt mit Spaß die Noten verbessern
und sofort Zugriff auf alle Inhalte erhalten!
30 Tage kostenlos testenInhaltsverzeichnis zum Thema
Einführung in die Thermodynamik
Die Thermodynamik und ihre drei Hauptsätze beschreiben physikalische Systeme und ihre Übergänge von einem Zustand in einen anderen. Zustände werden durch die Zustandsgrößen Temperatur, Volumen und Druck beschrieben, während die Übergänge durch die Prozessgrößen Wärme Q und Arbeit W charakterisiert sind. Führt man einem thermodynamischen System Wärme zu oder verrichtet es mechanische Arbeit, so ändert sich der Zustand dieses Systems.
Wärme Q und das Erwärmungsgesetz
Wird einem thermodynamischen System Wärme zugeführt, so erhöht sich dessen Temperatur. Aber nicht jeder Stoff erwärmt sich in der gleichen Weise. Wie viel Wärme einem Stoff zugeführt werden muss, damit sich ein Kilogramm des Stoffes um ein Kelvin erwärmt, ist durch die spezifische Wärmekapazität c gegeben:
$c=\frac{Q}{m\cdot\Delta T}$.
Dieser Zusammenhang gilt allerdings nur, solange sich der Aggregatzustand des Stoffes nicht ändert. Möchtest du den Umgang mit der Formel lernen, versuche dich doch einmal an Übungen zum Erwärmungsgesetz.
Arbeit W
Auch durch mechanische Arbeit kann sich der Zustand eines Systems ändern. Ein Beispiel ist die Volumenarbeit, wie sie in der technischen Anwendung häufig verwendet wird. Mit Hilfe der allgemeinen Gasgleichung und der Formel für den Druck lässt sich die Volumenarbeit herleiten:
$W=\int_{s_1}^{s_2} F(s) \text{d}s=nRT\ln{(\frac{V_1}{V_2})}$.
Anhand des Vorzeichens des Ergebnisses kannst du erkennen, ob die Arbeit vom System ($-$) verrichtet wird oder sie von außen hinzugeführt ($+$) wird.
Wärmekraftmaschine
Wärmekraftmaschinen funktionieren nach den thermodynamischen Gesetzen und verrichten Arbeit. Dabei wird der Maschine Wärme zugeführt, sodass diese Arbeit verrichtet und Abwärme abführt. Danach ist die Maschine wieder in ihrem Anfangszustand.
Solche thermodynamischen Kreisprozesse werden mit $V$-$p$-Indikatordiagrammen dargestellt. Die Darstellung erfolgt über eine Druck- und eine Volumenachse und über Isothermen. Die Fläche des Kreisprozesses entspricht der verrichteten Arbeit.
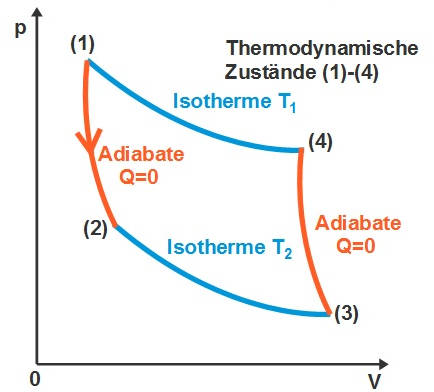
Da es sich nicht vermeiden lässt, dass ein Anteil der zugeführten Wärme ungenutzt bleibt, ist der thermische Wirkungsgrad stets kleiner als eins. Noch etwas kleiner ist der technische Wirkungsgrad, da es ebenfalls immer Reibungsverluste gibt.
$\eta_\text{therm}$: thermischer Wirkungsgrad.
$\eta_\text{tech}$: technischer Wirkungsgrad.
$\eta_{tech} \lt \eta_{therm} = \frac{T_1 - T_2}{T_2} \lt 1$
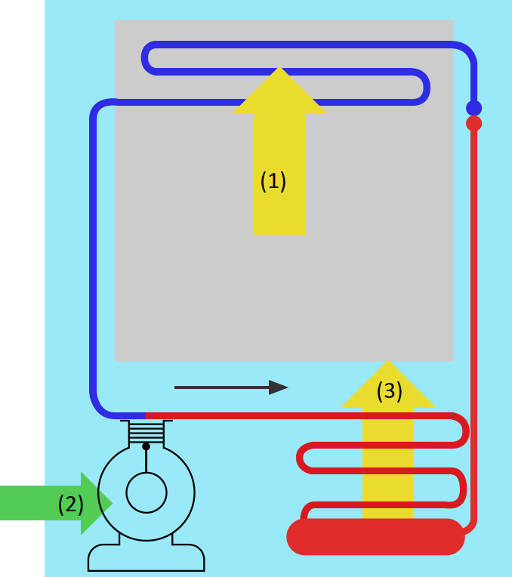
Das Gegenteil einer Wärmekraftmaschine ist die Wärmepumpe. Dabei verläuft der Kreisprozess in umgekehrte Richtung. Ein Beispiel ist der Kühlschrank. Dieser nutzt eine Flüssigkeit, die durch die Wärme der Lebensmittel verdampft wird (1). Die Lebensmittel verlieren so Energie und werden kälter. Ein Kompressor (2) komprimiert den Dampf so starkt, dass er flüssig wird. Dabei wird Verdunstungswärme abgegeben (3) und die kalte Flüssigkeit erneut in den Kühlschrank geschickt.
Beispiele für Wärmekraftmaschinen
Du wirst nun Beispiele aus der Technik kennenlernen. Es handelt sich zwar immer um eine Wärmekraftmaschine, die einzelnen Arbeitsschritte unterscheiden sich jedoch. Daher hier noch einige wichtige Begriffe:
- Adiabatisch bedeutet, dass das System keine Wärme mit seiner Umgebung austauscht.
- Isotherm bedeutet, dass der Übergang bei konstanter Temperatur stattfindet.
- Isochor bedeutet, dass der Übergang bei konstantem Volumen stattfindet.
- Isobar bedeutet, dass der Übergang bei konstantem Druck stattfindet.
Der Ottomotor
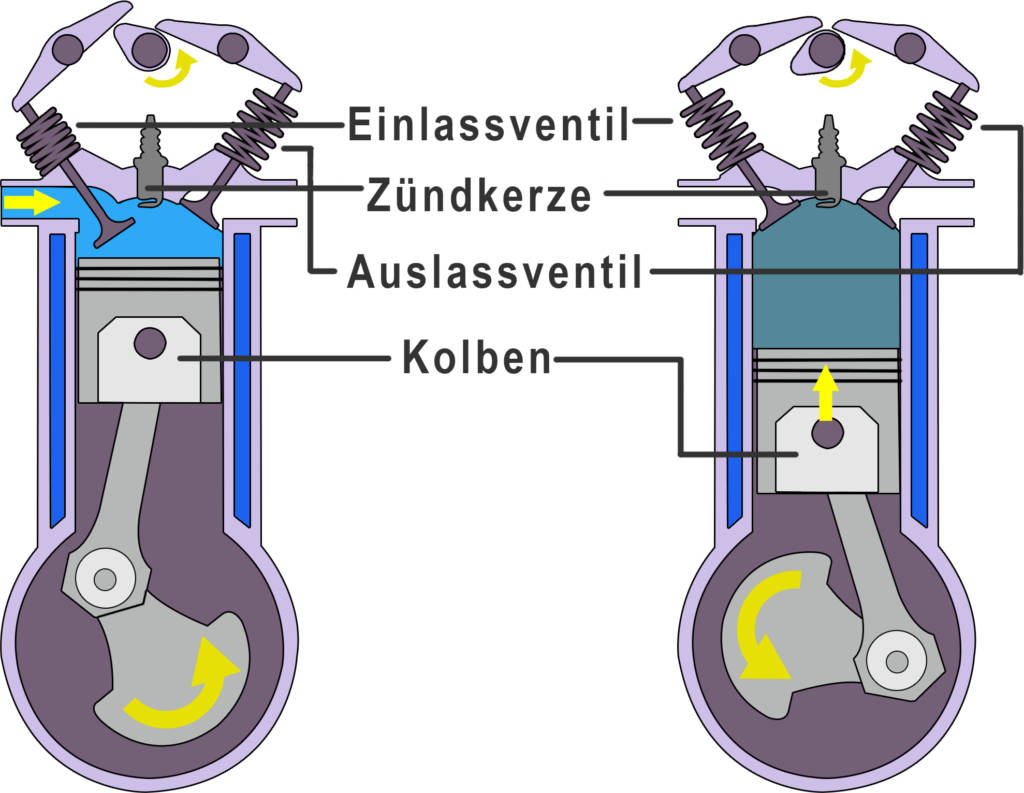
Der Ottomotor ist eine Verbrennungskraftmaschine und sorgt in vielen PKWs und Motorrädern für den Antrieb. Er arbeitet in vier Takten: Der 1. Takt beinhaltet das Ansaugen des Benzin-Luft-Gemischs in den Zylinder. Im 2. Takt wird das Gemisch adiabatisch komprimiert, sodass sich Druck und Temperatur erhöhen. Der 3. Takt ist der Arbeitstakt. Hier wird das Gemisch gezündet, verbrennt und dehnt sich aus. Diese Volumenarbeit wird vom Kolben schlussendlich an die Räder weitergegeben und sorgt für den Antrieb. Im 4. Takt wird das Abgas ausgestoßen. Mehr darüber lernst du in unserem Video: Ottomotor Aufbau
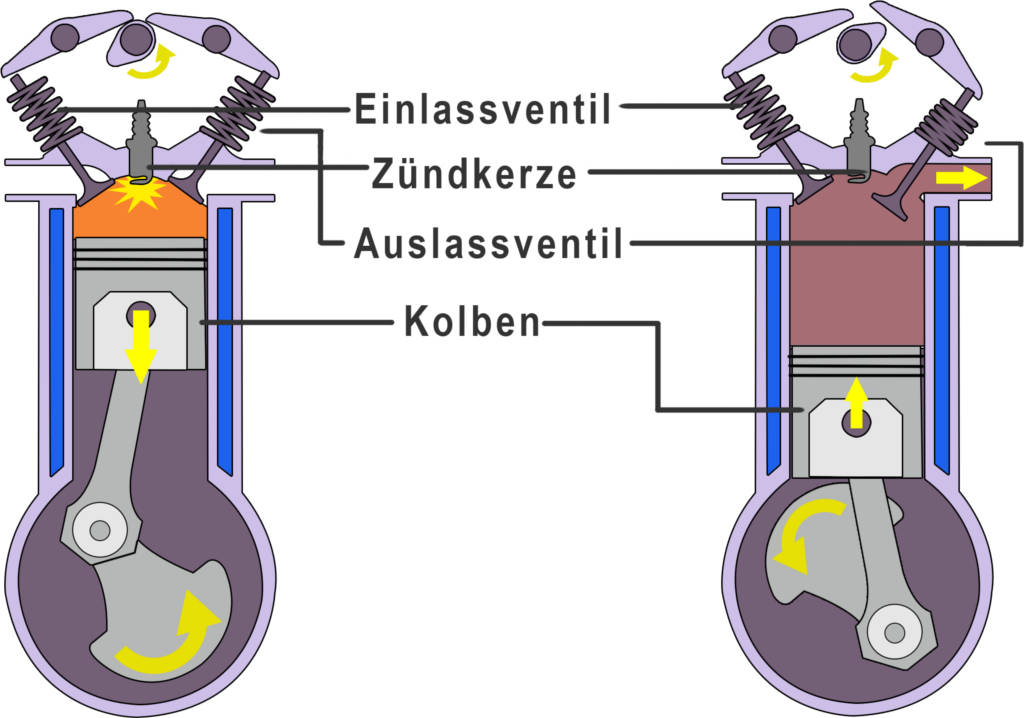
Der Dieselmotor
Der Dieselmotor findet ebenfalls Verwendung in PKWs, aber auch in Schiffen. Er arbeitet ähnlich wie der Ottomotor. Statt eines Luft-Treibstoff-Gemischs wird im Dieselmotor nur Luft angesaugt. Wird diese im zweiten Takt komprimiert, wird sie so heiß, dass sie den Kraftstoff, der jetzt eingespritzt wird, entzündet. Der Dieselmotor benötigt also keine Zündkerzen. Auch hier ist der dritte Takt der Arbeitstakt und der vierte stößt die Abgase aus.
Der Ottomotor genießt gegenüber des Dieselmotors einige Vorteile: Er ist günstiger, leistungsfähiger, leiser und produziert weniger Schadstoffe. Er hat aber auch Nachteile. Benzin ist gefährlicher als Diesel. Außerdem ist ein Dieselmotor effizienter und haltbarer.
Weitere Beispiele
Auch eine Gasturbine arbeitet mittels eines thermodynamischen Kreisprozesses. Die vier Takte sind adiabatische Kompression, isobare Wärmezufuhr durch den Wärmetauscher, adiabatische Expansion durch Verbrennung des Treibstoffes und isobare Wärmeabgabe des Abgases.
Der Sterlingmotor, der früher häufig gebaut wurde, nutzt isotherme Expansion, isochore Abkühlung, isotherme Kompression und isochore Erwärmung.
Doch wie ist der Aufbau des Elektromotors? Im Gegensatz dazu ist er kein thermodynamischer Kreisprozess.
Alle Videos und Lerntexte zum Thema
Videos und Lerntexte zum Thema
Thermische Energie und Wärmekraftmaschinen (14 Videos, 3 Lerntexte)
Alle Arbeitsblätter zum Thema
Arbeitsblätter zum Thema
Thermische Energie und Wärmekraftmaschinen (7 Arbeitsblätter)
-
 Ausdehnungsarbeit und erster Hauptsatz
PDF anzeigen
Ausdehnungsarbeit und erster Hauptsatz
PDF anzeigen -
 Erwärmungsgesetz (Übungsvideo)
PDF anzeigen
Erwärmungsgesetz (Übungsvideo)
PDF anzeigen -
 Arten von Wärmekraftmaschinen
PDF anzeigen
Arten von Wärmekraftmaschinen
PDF anzeigen -
 Energieumwandlung im Verbrennungsmotor
PDF anzeigen
Energieumwandlung im Verbrennungsmotor
PDF anzeigen -
 Ottomotor – Aufbau und Funktion
PDF anzeigen
Ottomotor – Aufbau und Funktion
PDF anzeigen -
 Dieselmotor – Aufbau und Funktion
PDF anzeigen
Dieselmotor – Aufbau und Funktion
PDF anzeigen -
 Kältemaschine und Wärmepumpe
PDF anzeigen
Kältemaschine und Wärmepumpe
PDF anzeigen
Beliebteste Themen in Physik
- Temperatur
- Schallgeschwindigkeit
- Dichte
- Drehmoment
- Transistor
- Lichtgeschwindigkeit
- Elektrische Schaltungen – Übungen
- Galileo Galilei
- Rollen- Und Flaschenzüge Physik
- Radioaktivität
- Aufgaben zur Durchschnittsgeschwindigkeit
- Lorentzkraft
- Beschleunigung
- Gravitation
- Ebbe und Flut
- Hookesches Gesetz Und Federkraft
- Elektrische Stromstärke
- Elektrischer Strom Wirkung
- Reihenschaltung
- Ohmsches Gesetz
- Freier Fall
- Kernkraftwerk
- Reflexionsgesetz: Ebener Spiegel – Übungen
- Was sind Atome
- Aggregatzustände
- Infrarot, Uv-Strahlung, Infrarot Uv Unterschied
- Isotope, Nuklide, Kernkräfte
- Transformator
- Lichtjahr
- Si-Einheiten
- Fata Morgana
- Gammastrahlung, Alphastrahlung, Betastrahlung
- Kohärenz Physik
- Mechanische Arbeit
- Schall
- Elektrische Leistung
- Dichte Luft
- Ottomotor Aufbau
- Kernfusion
- Trägheitsmoment
- Heliozentrisches Weltbild
- Energieerhaltungssatz Fadenpendel
- Linsen Physik
- Ortsfaktor
- Interferenz
- Diode und Photodiode
- Wärmeströmung (Konvektion)
- Schwarzes Loch
- Frequenz Wellenlänge
- Elektrische Energie





























