Monosaccharide
Entdecke die Welt der Monosaccharide: Sie sind Einfachzucker und essentielle Bausteine von DNA und RNA. Sie zeichnen sich durch ihre Festigkeit, Farblosigkeit, Wasserlöslichkeit und Brennbarkeit aus. In Lebensmitteln findet man sie häufig, und sie liefern wertvolle Energie. Hier erfährst du, wie kein Zucker dem anderen gleicht!
in nur 12 Minuten? Du willst ganz einfach ein neues
Thema lernen in nur 12 Minuten?
-
 5 Minuten verstehen
5 Minuten verstehen
Unsere Videos erklären Ihrem Kind Themen anschaulich und verständlich.
92%der Schüler*innen hilft sofatutor beim selbstständigen Lernen. -
 5 Minuten üben
5 Minuten üben
Mit Übungen und Lernspielen festigt Ihr Kind das neue Wissen spielerisch.
93%der Schüler*innen haben ihre Noten in mindestens einem Fach verbessert. -
 2 Minuten Fragen stellen
2 Minuten Fragen stellen
Hat Ihr Kind Fragen, kann es diese im Chat oder in der Fragenbox stellen.
94%der Schüler*innen hilft sofatutor beim Verstehen von Unterrichtsinhalten.

Grundlagen zum Thema Monosaccharide
Monosaccharide in der Chemie
Zucker kennt jeder. Aber wusstest du, dass es viele verschiedene Zuckerarten gibt? Chemisch betrachtet ist Zucker nicht gleich Zucker. In diesem Text lernst du die Monosaccharide kennen. Diese begegnen dir im Alltag ständig. Du findest sie beispielsweise in verschiedenen Lebensmitteln, aber sie sind auch Bestandteil unserer Nukleinsäuren – der DNA und der RNA. Aber was genau sind Monosaccharide?
Monosaccharide sind Einfachzucker, die zur Stoffklasse der Kohlenhydrate gehören. Monosaccharide sind die Bausteine von Disacchariden (Zweifachzucker) und Polysacchariden (Vielfachzucker).
Ein wichtiges Merkmal von Monosacchariden ist, dass sie entweder eine Aldehyd- $\left( \ce{-CHO} \right)$ oder eine Keto-Gruppe $\left( \ce{-C=O} \right)$ enthalten. Mit Aldehyden und Ketonen solltest du dich also bereits auskennen, um dem nachfolgenden Text besser folgen zu können.
Wusstest du schon?
Monosaccharide sind die Bausteine des Zuckers! Glucose, ein bekanntes Monosaccharid, ist die Hauptenergiequelle für deinen Körper. Wenn du zum Beispiel ein Stück Obst isst, wird die darin enthaltene Glucose schnell in Energie umgewandelt, die du fürs Denken, Bewegen und sogar fürs Atmen benötigst!
Monosaccharide – Eigenschaften
Alle Monosaccharide sind unter Normalbedingungen fest, farblos und gut wasserlöslich. Außerdem sind sie brennbar, liefern also Energie. Die Einfachzucker haben außerdem eine höhere Dichte als Wasser.
Monosaccharide – Aufbau
Monosaccharide bzw. ihre Moleküle können als Kohlenstoffring oder Kohlenstoffkette vorliegen. Der Aufbau der Monosaccharide lässt sich am einfachsten in der Kettenform beschreiben. Dabei sind die Kohlenstoffatome untereinander über Einfachbindungen verbunden und tragen jeweils noch funktionelle Gruppen. Alle Einfachzucker sind mehrfache, genauer gesagt mehrwertige Alkohole, sie besitzen also mehrere Hydroxygruppen $\left( \ce{-OH} \right)$. Unterschieden werden die Monosaccharide nach der Anzahl der Kohlenstoffatome und der zusätzlichen funktionellen Gruppen:
| Name | Summenformel | Anzahl der Kohlenstoffatome | Funktionelle Gruppe |
|---|---|---|---|
| Ribose | $\ce{C5H10O5}$ | 5 | Aldehydgruppe |
| Glucose | $\ce{C6H12O6}$ | 6 | Aldehydgruppe |
| Fructose | $\ce{C6H12O6}$ | 6 | Ketogruppe |
| Galactose | $\ce{C6H12O6}$ | 6 | Aldehydgruppe |
Ist das Monosaccharid aus fünf Kohlenstoffatomen aufgebaut, wird es als Pentose bezeichnet, bei sechs Kohlenstoffatomen als Hexose.
Wenn bei der funktionellen Gruppe eine Aldehydgruppe ($\ce{-CHO}$) vorliegt, bezeichnet man diese Monosaccharide als Aldosen. Handelt es sich um eine Ketogruppe ($\ce{-CO}$), spricht man von Ketosen.
Ribose, Glucose, Fructose und Galactose sind also nur Trivialnamen. Ribose kann beispielsweise auch als Pentose oder Aldose bezeichnet werden, da das Molekül über fünf Kohlenstoffatome und eine Aldehydgruppe verfügt.
Kontrovers diskutiert:
Wissenschaftlerinnen und Wissenschaftler sind sich uneinig, ob der Verzehr von Monosacchariden in natürlichen Lebensmitteln wie Obst wirklich gesünder ist als der Konsum von industriell hergestelltem Zucker.
Einige Forscherinnen und Forscher betonen die Vorteile von Vitaminen und Ballaststoffen in Früchten, während andere argumentieren, dass Zucker grundsätzlich Zucker bleibt, unabhängig von der Quelle. Was denkst du?
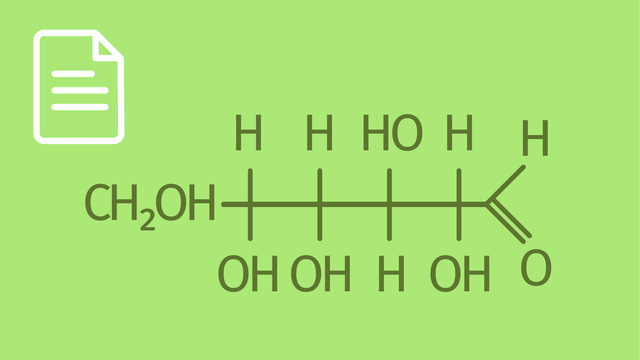
Wie du aus der Tabelle außerdem entnehmen kannst, ist die Unterscheidung der verschiedenen Einfachzucker nach der Summenformel nicht immer möglich (vgl. Glucose und Galactose). Dazu muss die Strukturformel betrachtet werden. Aus dieser wird erst ersichtlich, welche funktionellen Gruppen vorliegen und v. a. welche Stellung diese an den Kohlenstoffatomen haben:
Wir haben hier der Einfachheit halber nur die linearen Moleküle dargestellt. Wie bereits erwähnt, können Einfachzucker auch Ringe bilden. So könnten alle drei dargestellten Moleküle auch als geschlossener Ring aus sechs $\ce{C}$-Atomen vorliegen. In der linearen Darstellung ist aber gut erkennbar, dass beispielsweise der Unterschied zwischen Glucose und Galactose einzig in der Stellung der Hydroxygruppe $\left( \ce{-OH} \right)$ am vierten $\ce{C}$-Atom (von oben gezählt) liegt.
Fehleralarm
Nicht alle Monosaccharide haben die gleiche Form. Es gibt sowohl lineare als auch ringförmige Strukturen von Monosacchariden. Ringbildungen sind in wässrigen Lösungen am häufigsten.
Die Chemie der Einfachzucker wird also von der Anzahl der Kohlenstoffatome, den funktionellen Gruppen und auch von der Struktur des Moleküls bestimmt.
Monosaccharide – Beispiele und Vorkommen
Die wichtigsten Monosaccharide sind die zuvor schon genannten: Ribose, Glucose, Fructose und Galactose.
Glucose, Fructose und Galactose werden mit der Nahrung aufgenommen. Sie können über Schleimhäute direkt ins Blut geleitet werden und dienen im Organismus über den Prozess der Zellatmung der Energiegewinnung.
Glucose (auch Traubenzucker genannt) und Galactose führen zu einem direkten Anstieg des Blutzuckerspiegels, liefern also schnell Energie. Glucose bildet außerdem den Grundbaustein von Stärke. Stärke findet sich beispielsweise in Kartoffeln und Getreiden.
Fructose ist in Obst als Fruchtzucker enthalten und bildet in Verbindung mit Glucose das Disaccharid Saccharose, unseren Haushaltszucker.
Galactose ist in Verbindung mit Glucose Bestandteil des Milchzuckers Lactose.
Ribose ist ein wichtiger struktureller Bestandteil der RNA, die eine große Rolle bei der Übertragung und Verarbeitung genetischer Informationen (also der DNA) in unseren Zellen spielt.
Schlaue Idee
Achte auf die Zutatenliste bei Lebensmitteln. Produkte mit hohem Anteil an Glucose oder Fructose können dir kurzfristig Energie geben, sind aber in größeren Mengen nicht gesund.
Ausblick – das lernst du nach Monosaccharide
Was passiert, wenn sich Monosaccharide verbinden? Finde es heraus, indem du dich auch mit Disacchariden, Polysacchariden und der glykosidischen Bindung in Kohlenhydraten beschäftigst. Vertiefe dein chemisches Verständnis und setze die Erforschung der Zuckerchemie fort!
Zusammenfassung der Monosaccharide
- Monosaccharide sind Einfachzucker. Sie gehören zur Stoffklasse der Kohlenhydrate. Das wesentliches Merkmal ihrer Moleküle ist, dass sie mehrwertige Alkohole mit einer zusätzlichen funktionellen Gruppe (Aldehyd- oder Keto-Gruppe) sind.
- Monosaccharide mit Aldehyd-Gruppe sind Aldosen, solche mit Keto-Gruppe sind Ketosen.
- Aldosen und Ketosen können sich außerdem in der Anzahl der Kohlenstoffatome, der Stellung der Hydroxygruppen und damit allgemein in der Molekülstruktur unterscheiden.
- Die Moleküle der Einfachzucker können linear oder ringförmig vorliegen. Zwei Monosaccharide können sich zu einem Disaccharid (z. B. Saccharose) verbinden oder noch längere Ketten, sogenannte Polysaccharide (z. B. Stärke), bilden.
- Die wichtigsten Monosaccharide sind Ribose, Glucose, Fructose und Galactose. Glucose ist der wichtigste Energielieferant im menschlichen Körper.
Häufig gestellte Fragen zum Thema Monosaccharide
Transkript Monosaccharide
Guten Tag und herzlich willkommen. Dieses Video heißt Monosaccharide. Der Film gehört zur Reihe Kohlenhydrate. An Vorkenntnissen solltet Ihr gut wissen, was Alkohole, Aldehyde und Ketone sind. Das Ziel des Videos ist ein erster Einstieg in das Thema. Der Film besteht aus 7 Abschnitten. 1. Teil der Kohlehydrate 2. Chemische Zuordnung 3. Einteilung 4. Eigenschaften 5. Vorkommen 6. Nachweis und 7. Ernährung
Teil der Kohlehydrate Carl Schmidt prägte 1844 für eine neue Verbindungsklasse einen Namen, er nannte bestimmte Verbindungen Kohlenhydrate. Man konnte nämlich durch das Experiment zeigen, dass sich diese Stoffe in Kohlenstoff und Wasser zerlegen lassen. Die Vorstellung dass diese Stoffe, nur aus Kohlenstoff und Wasser zusammengesetzt, bestehen, erwies sich als falsch. Der Name Kohlenhydrate blieb jedoch bis heute erhalten und wird weiter benutzt. Gewöhnlich wird die Stoffklasse der Kohlenhydrate folgendermaßen unterteilt. In Monosaccharide, das sind Einfachzucker, Disaccharide, das sind Zweifachzucker und Polysaccharide, das sind Vielfachzucker. Monosaccharide sind die Bausteine von Disacchariden und Polysacchariden. Diese Bausteine kann man sich vereinfacht so vorstellen. Es handelt sich hier um Monosaccharide und zwar in schematischer Darstellung. 2 solcher Bausteine, 2 Monosaccharid-Moleküle, bilden ein Disaccharid-Molekül. Auch das ist schematisch dargestellt. Viele Monosaccharid Moleküle bilden eine lange Polysaccharid-Kette. Auch diese Darstellung ist schematisch.
Chemische Zuordnung Monosaccharide können als Ringe oder Ketten auftreten. Als Ringe trifft man sie häufiger an. Für einen Einstieg betrachten wir jedoch nur die Ketten. Am Ende der Kohlenstoffkette sitzt eine funktionelle Gruppe CHO. Neben den Wasserstoffatomen findet man noch mehrere gleiche funktionelle Gruppen OH. Monosaccharide sind somit Mehrfachalkohole. Diese Mehrfachalkohole sind gleichzeitig auch ein Aldehyd. Es besteht aber auch noch eine zweite Möglichkeit. Wieder haben wir einen Mehrfachalkohol. Außerdem hat das Molekül noch eine andere funktionelle Gruppe. Kennt Ihr sie? Wenn nicht, so sage ich es Euch. Es ist die Ketogruppe, also oder Keton. Daher kann ein Monosaccharid auch ein Keton sein.
Einteilung Die Unterteilung der Monosaccharide ist zum einen nach der Zahl der Kohlenstoffatome möglich. Ich möchte für die Zahl n den Namen nennen und in einigen Fällen Beispiele angeben. 3 Kohlenstoffatome, das ist eine Triose. 4 Kohlenstoffatome, Tetrose. 5 Kohlenstoffatome: Pentose. Ribose ist ein Beispiel. Wir werden von ihr noch sprechen. 6 Kohlenstoffatome: Hexose. Glucose, Fructose und Galactose sind Beispiele. Wir werden über sie noch sprechen. Eine 2. Möglichkeit der Einteilung besteht nach funktioneller Gruppe. Wir haben bereits gelernt, dass ein Monosaccharid eine Aldehyd-Gruppe oder eine Keto-Gruppe enthalten kann. Im ersten Fall sprechen wir von einer Aldose. Im 2. Fall von einer Ketose. Glucose ist eine Aldose, Fructose eine Ketose. Außerdem kann man Monosaccharide nach dem Ring unterscheiden. Ein Sechsring mit einem Sauerstoffatom heißt Pyranose. Ein Fünfring mit einem Sauerstoffatom heißt Furanose.
Eigenschaften Monosaccharide sind fest. Sie sind farblos. Monosaccharide sind brennbar. Sie liefern viel Energie. Im Wasser fallen sie zunächst nach unten. Sie haben eine höhere Dichte als Wasser. Schon bald sind sie aufgelöst. Sie sind sehr gut wasserlöslich.
Vorkommen Die Ribose, erinnert Euch, hat 5 Kohlenstoffatome. Sie ist Baustein einer Nukleinsäure, der RNS, und somit auch für die Vererbung zuständig. Ihr könnt sie gut erkennen. Es sind jeweils die Fünfringe mit einem Sauerstoffatom. Die Glucose, erinnert Euch, hat 6 Kohlenstoffatome. Man nennt sie auch Traubenzucker. Entdeckt wurde Glucose in einer Weinrebe. In der Gerste ist Glucose der Baustein des Malzzuckers. Sie ist Stärkebaustein. Stärke ist ein Polysaccharid. Fructose nennt man auch Fruchtzucker. Sie ist ein Baustein unseres Zuckers. Man nennt ihn auch Rohrzucker oder Rübenzucker. Das ist ein Disaccharid. Weniger bekannt aber auch sehr wichtig ist die Galactose. Man nennt sie auch Schleimzucker. Galactose finden wir in der Milch. Zusammen mit Glucose bildet sie die Lactose, den Milchzucker. Das ist ein Disaccharid.
Nachweise Glucose kann man mit der Fehling-Probe nachweisen. Dabei entsteht aus blauen Kupferionen rotes Kupfer-1-Oxid. Der zweite Nachweis erfolgt nach Tollens. Aus Silberionen entsteht ein Silberspiegel. Fructose wird anders nachgewiesen. Man löst in Wasser, gibt Säure dazu, dann Resorcin, eine organische Verbindung und erwärmt. Es entsteht ein roter Niederschlag. Das ist die Seliwanow-Probe.
Ernährung Zucker spielen eine große Rolle bei unserer Ernährung. Monosaccharide können direkt vom Magen über den Darm in das Blut gelangen. Di- und Polysaccharide hingegen nicht. Dabei zeigen Glucose und Galactose noch eine besondere Wirkung. Sie sind die einzigen Monosaccharide, die zu einem direkten Anstieg des Blutzuckers führen. Dieses Wissen ist wichtig für Diabetiker. Kohlenhydrataufnahme kann verschieden erfolgen. Durch Zucker bestehend aus Mono- und Disacchariden. Man findet sie in Honig, Süßigkeiten und Früchten. Oder man nimmt Stärke auf. Das sind Polysaccharide, enthalten in Reis, Mais und Kartoffeln. Es wird empfohlen, höchstens 10 Prozent Mono- und Disaccharide und mindestens 90 Prozent Polysaccharide aufzunehmen.
Ich danke für die Aufmerksamkeit. Alles Gute! Auf Wiedersehen!
Monosaccharide Übung
-
Beschreibe die Monosaccharide.
TippsLösungMonosaccharide sind Einfachzucker. Sie liegen am häufigsten in Ringform vor, können aber auch kettenförmig sein. Die Moleküle bestehen in der Mitte aus einem Kohlenstoffgerüst. An diesem befinden sich neben Wasserstoffatomen auch mehrere Hydroxid-Gruppen $\left(\ce{-OH} \right)$. Daher können Einfachzucker auch als Mehrfachalkohole bezeichnet werden. Sie können weiterhin als Aldehyde oder Ketone vorliegen. Dies ist abhängig von der im Molekül befindlichen funktionellen Gruppe. Ein Keton trägt eine Keto-Gruppe $\left(\ce{-C=O} \right)$ und ein Aldehyd eine Aldehyd-Gruppe $\left(\ce{-CHO} \right)$.
Monosaccharide sind fest, gut in Wasser lösbar und farblos. Die Löslichkeit in Wasser ist zum Beispiel wichtig für den Transport von Monosacchariden im Blut.
-
Gib die Einteilung der Monosaccharide wieder.
TippsIn einem Ring werden die Kohlenstoffatome nicht eingetragen. Jede Ecke steht für ein $\ce{C}$-Atom. Für andere Elemente wird das entsprechende Symbol eingetragen.
LösungUm Monosaccharide zu benennen, gibt es drei Möglichkeiten. Bei der ersten wird die Anzahl der $\ce{C}$-Atome bestimmt. Für diese Zahl wird ein entsprechendes Zahlwort an den Anfang des Namens gesetzt und mit -ose ergänzt. Für drei Kohlenstoffatome setzt man tri an den Anfang des Namens. Somit ergibt sich Triose als Lösung. Ein Zucker mit 4 $\ce{C}$-Atomen nennt man Tetrose, mit 5 $\ce{C}$-Atomen Pentose und mit 6 $\ce{C}$-Atomen Hexose. Glucose, Fructose oder Galactose währen ein Beispiel für eine Hexose.
Bei der zweiten Methode nutzt man die funktionellen Gruppen. Aldehyde besitzen die Aldehyd-Gruppe. Sie muss am Ende einer Kohlenstoffkette stehen. Der Grund hierfür liegt in der Vierbindigkeit des Kohlenstoffatoms. Am $\ce{C}$-Atom der Gruppe sitzt ein $\ce{H}$-Atom und ein $\ce{O}$-Atom ist mit diesem über eine Doppelbindung verbunden. Somit kann das $\ce{C}$-Atom nur noch eine Bindung eingehen, und zwar zu einem anderen Kohlenstoffatom. Trägt ein Monosaccharid diese Gruppe, so nennt man es Aldose. Die Keto-Gruppe gibt den Ketosen ihren Namen. Sie setzt sich zusammen aus einem $\ce{C}$-Atom und einem $\ce{O}$-Atom, das über eine Doppelbindung mit ersterem verbunden ist. Keto-Gruppen stehen nicht am Anfang/Ende einer Kohlenstoffkette, sondern innerhalb dieser.
Die Ringe der Monosaccharide werden in der letzten Methode betrachtet. In einem Sechsring kann man 6 Ecken zählen. Dabei sind fünf von diesen mit $\ce{C}$-Atomen besetzt und eine mit einem $\ce{O}$-Atom. Einen solchen Zucker nennt man Pyranose. Ein Fünfring hat 5 Ecken, von denen 4 mit $\ce{C}$-Atomen besetzt sind und eine mit einem $\ce{O}$-Atom besetzt ist. Diese Zucker nennt man Furanose. In den Ringen müssen die Kohlenstoffatome in den Ecken und ihre dazugehörigen Wasserstoffatome nicht geschrieben werden. Nur andere Atome, wie Sauerstoff oder Stickstoff, werden entsprechend eingetragen.
-
Erarbeite die Namen der Monosaccharide.
TippsDas Zahlwort für 3 ist tri.
Monosaccharide tragen im letzten Namensteil immer die Endung -ose.
LösungIn Bild 1 ist die Anzahl ($n$) der Kohlenstoffatome dargestellt. Die Methode der Einteilung der Einfachzucker verläuft nach Zahl der Kohlenstoffatome. Verbindung 1 soll 6 $\ce{C}$-Atome besitzen. Das Zahlwort dazu lautet „hex“. Hängt man nun noch die Endung -ose heran, dann erhält man den Namen des Zuckers: Hexose. Die zweite Verbindung hat 8 $\ce{C}$-Atome. Hierzu lautet das Zahlwort "oct". Mit der Endung -ose ergibt sich auch hier der Name des Einfachzuckers: Octose.
Die Moleküle in Bild 2 unterschieden sich in der Anzahl der $\ce{C}$-Atome und in den funktionellen Gruppen. Somit kommt hier die Methode nach funktionellen Gruppen zur Anwendung. In Verbindung (a) sitzt die Gruppe am Ende der Kohlenstoffkette. Weiterhin besteht diese Gruppe aus einem $\ce{C}$-, einem $\ce{H}$- und einem $\ce{O}$-Atom. Es handelt sich also um eine Aldehyd-Gruppe und das Monosaccharid ist eine Aldose. Verbindung (b) trägt die funktionelle Gruppe innerhalb der Kohlenstoffkette. Sie besteht aus einem $\ce{C}$- und einem $\ce{O}$-Atom. Da dies die Keto-Gruppe ist, nennt sich der Einfachzucker Ketose.
-
Erkläre die Seliwanow-Probe mit Hilfe von Reaktionsgleichungen.
TippsNutze die unvollständigen Wortgleichungen, um einige Edukte und Produkte zu enthalten.
Es ist richtig ausgeglichen, wenn auf beiden Seiten des Reaktionspfeils die gleiche Anzahl der jeweiligen Atome steht.
Nutze falls nötig einen Notizzettel beim Zählen der Atome.
LösungAus der ersten Wortgleichung ist das Edukt und eines der Produkte zu entnehmen. Die Ketose ist in diesem Fall unsere Fructose mit der Summenformel $\ce{C6H12O6}$. Das erste Produkt ist bereits vorgegeben als $\ce{C6H6O3}$. Auf den ersten Blick ist zu erkennen, dass die Anzahl der $\ce{C}$-Atome gleich ist. Jedoch fehlen auf Seiten der Produkte $\ce{6 H}$-Atome und $\ce{3 O}$-Atome. Mit Hilfe dieser Zahlen und der Wortgleichung (es wird Wasser abgespalten) ergibt sich die Lösung: $\ce{3 H2O}$.
Bei der zweiten Teilreaktion soll das Produkt von eben mit Sauerstoff $\left( \ce{O2} \right)$ und Resorcin weiter reagieren. Die Summenformel von letzterem ist dabei bereits vorgegeben und die Summenformel des Produktes aus Gleichung 1 hat die Formel $\ce{C6H6O3}$. Eines der Produkte der zweiten Reaktion ist bereits angegeben: der rote Farbstoff $\left( \ce{C18H12O5} \right)$. Als weiteres Produkt entsteht Wasser $\left( \ce{H2O} \right)$. Um zu wissen, wie viel $\text{mol}$ davon entstehen, betrachten wir die Anzahl an $\ce{O}$- und $\ce{H}$-Atomen. Dabei muss bedacht werden, dass die noch unklar ist, wie viel $\text{mol}$ Sauerstoff an der Reaktion beteiligt sind. Somit muss die Menge an Wasser mit Hilfe der Wasserstoffatome bestimmt werden. Links vom Reaktionspfeil sind $18$ Atome zu zählen und rechts $12$. Daraus ergibt sich eine Differenz von $6$ Atomen. Ein Wassermolekül hat $\ce{2 H}$-Atome. Folglich entstehen $3\,\text{mol}$ Wasser $\left( \ce{3 H2O} \right)$. Nun kann die Menge an Sauerstoff auf Seiten der Edukte bestimmt werden. Rechts vom Reaktionspfeil sind $\ce{8 O}$-Atome und links $7$, womit sich eine Differenz von $1$ ergibt. Da Sauerstoff zweiatomig vorliegt, muss die Differenz durch zwei geteilt werden. Die Lösung ist somit $0{,}5\,\ce{O2}$.
-
Erkenne, in welchen Lebensmittel folgende Saccharide enthalten sind.
TippsIn Stärke finden sich Polysaccharide.
LösungMonosaccharide sind Einfachzucker. Zu ihnen gehören zum Beispiel Glucose, Fructose und Galactose. Glucose und Galactose haben eine besondere Wirkung auf den menschlichen Körper: Sie sorgen für einen direkten Anstieg des Blutzuckerspiegels. Disaccharide sind Zweifachzucker. Der wirtschaftlich wichtigste Vertreter ist die Saccharose (Rohr- und Rübenzucker). Mono- und Disaccharide sind enthalten in Früchten (Erdbeeren, Äpfeln, Bananen,...), in Honig und in vielen Süßigkeiten (Bonbons, Kuchen, Lollipops,...). Empfohlen wird eine tägliche Aufnahme dieser Zucker von unter $10\,\%$.
Neben Stärke sind auch Pektine und Cellulose Beispiele für Polysaccharide. Sie setzten sich zusammen aus mehreren Monosacchariden. Polysaccharide sind in Kartoffeln, Mais oder Reis enthalten. Mindestens $90\,\%$ der täglichen Nahrung sollen diese Zucker ausmachen.
-
Erarbeite die Reaktionsgleichungen für den Nachweis von Glucose.
TippsEs ist richtig ausgeglichen, wenn auf beiden Seiten des Reaktionspfeils die jeweils gleiche Anzahl der Atome steht.
LösungBei der ersten Reaktion entsteht ein rot-brauner Niederschlag. Der Glucose-Nachweis erfolgt hier also mittels Fehling-Reagenz. Die ersten Lücken bei der Reaktionsgleichung der Oxidation lassen sich mithilfe des dazugehörigen Satzes füllen. Zu den Edukten gehört eine Verbindung mit einer Aldehyd-Gruppe. In diesem Fall ist es die Glucose, welche in abgekürzter Schreibweise eingetragen werden muss: $\ce{R-CHO}$. Wird diese funktionelle Gruppe oxidiert, dann entsteht eine Carbonsäure. Als ein Produkt muss also $\ce{R-COOH}$ eingetragen werden. Vergleicht man nun die Anzahl der Atome auf Produkt- und Eduktseite, dann fällt auf, dass auf Seiten der Produkte zwei $\ce{H}$- und ein $\ce{O}$-Atom fehlen. Es muss sich somit als drittes Produkt Wasser $\left( \ce{H2O} \right)$ bilden.
Die in der ersten Reaktion gebildeten Elektronen kommen bei der Reduktion zum Einsatz. Sie reagieren mit $\ce{2 Cu^{2+}}$ und Hydroxidionen. Das dabei entstehende Produkt <nobr>Kupfer(I)-hydroxid</nobr> hat die Summenformel $\ce{CuOH}$. Links vom Reaktionspfeil befinden sich allerdings zwei Kupferionen. Damit auf beiden Seiten gleich viele $\ce{Cu}$-Atome stehen, muss als Lösung $\ce{2 CuOH}$ eingetragen werden. Auf der Produktseite befinden sich nun zwei $\ce{O}$- und zwei $\ce{H}$-Atome. Somit müssen $2\,\text{mol}$ Hydroxidionen $\left( \ce{2 OH^-} \right)$ als Edukt eingesetzt werden. Das im letzten Schritt gebildete <nobr>Kupfer(I)-oxid</nobr> besitzt die Summenformel $\ce{Cu2O}$. Da hier zwei Kupferatome enthalten sind, müssen auf der Eduktseite ebenfalls zwei Kupferatome stehen. Die richtige Lösung ist somit $\ce{2 CuOH}$.
Beim zweiten Nachweis bildet sich ein Silberspiegel aus. Daher kommt hier das Tollens-Reagenz zur Anwendung. Im ersten Schritt wird die Aldehyd-Gruppe erneut zur Carboxyl-Gruppe oxidiert. Als Lösung bei den Produkten muss somit $\ce{R-COOH}$ in die Lücke eingesetzt werden. Als Edukt müssen auch bei dieser Oxidationsreaktion Hydroxidionen eingetragen werden. Um festzustellen, wie viele Mol benötigt werden, zählt man die $\ce{H}$- und $\ce{O}$-Atome auf beiden Seiten des Reaktionspfeils. Rechts sind je $3$ Atome zu zählen und links je $1$ Atom. Es müssen somit $\ce{2 OH^-}$ als Lösung auf der Eduktseite eingetragen werden.
Durch die anschließende Reduktion bildet sich der Silberspiegel, d. h. es bildet sich Silber $\left( \ce{Ag} \right)$. Bei der Reduktion kommt es zur Aufnahme von Elektronen. Somit sind Silberionen die Edukte dieser Reaktion. Da zwei Elektronen in der Oxidation gebildet wurden und Silberionen $\left( \ce{Ag^+} \right)$ die Ladung $1+$ tragen, muss als Lösung auf der Eduktseite $\ce{2 Ag^+}$ eingesetzt werden. Damit ergeben sich als Produkt $2\,\text{mol}$ Silber $\left( \ce{2 Ag} \right)$.

Grundbaustoffe der Nahrung – Kohlenhydrate, Eiweiße und Fette

Monosaccharide

Glucose und Fructose

Glucose – Kette oder Ring?

Monosaccharide mit 3 bis 6 C-Atomen

Monosaccharide – Nomenklatur und Stereochemie

Monosaccharide – Eigenschaften und Reaktionen

Pyranosen und Furanosen

D-Ribopyranose und D-Ribofuranose

Sesselform-Schreibweise der Pyranosen

Halbacetal- und Acetalbildung

Disaccharide

Disaccharide – Besondere Glykoside

Reduzierende und nichtreduzierende Disaccharide

Saccharose und Maltose

Polysaccharide

Polysaccharide – Cellulose, Stärke, Glykogen

Stärke und Cellulose

Nachweis von Kohlenhydraten

Moleküldarstellungen von Kohlenhydraten

Zuckerderivate
Glykoside und glykosidische Bindung

Glykolipide und Glykoproteine

Hyaluronsäure, Heparin, Chitin
10.352
sofaheld-Level
6.600
vorgefertigte
Vokabeln
8.340
Lernvideos
38.677
Übungen
33.886
Arbeitsblätter
24h
Hilfe von Lehrkräften

Inhalte für alle Fächer und Klassenstufen.
Von Expert*innen erstellt und angepasst an die Lehrpläne der Bundesländer.
Testphase jederzeit online beenden
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Ethansäure
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Polyurethan
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- fraktionierte Destillation
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte



 5 Minuten verstehen
5 Minuten verstehen
 5 Minuten üben
5 Minuten üben
 2 Minuten Fragen stellen
2 Minuten Fragen stellen

 Bereit für eine echte Prüfung?
Bereit für eine echte Prüfung?











Super Video Danke :)
Um ein Fach zu erklären, muss man es sehr mögen. Das ist nicht hinreichend, aber notwendig.
Ansonsten vielen Dank für das Lob.
Alles Gute und viel Erfolg
endlich ein Lehrer der ...ach endlich ein Lehrer bei dem das lernen nicht nur Spaß macht ; Nein - endlich versteht man auch was von dem Fach Chemie auch wenn die Vermutung nahe liegt man wüde sich das blos einbilden tut diese Annahme furchtbar gut. Besten Dank für diese Leistung.
war sehr gut danke
Gerne wieder!